서론
건강기능식품은 영양소 기능, 생리활성 기능, 그리고 질병 발생 위험 감소 기능과 같이 인체의 구조 및 기능에 유용한 효과를 줄 수 있는 원료나 성분을 제조 가공한 식품으로 정의된다[1]. 국민들의 소득수준의 향상과 로하스(LOHAS) 및 웰빙 추구를 통한 삶의 질적 향상 욕구가 증가되면서 건강기능식품에 대한 관심도 꾸준히 증가되고 있다. 특히 고령화 사회 진입에 따른 자가 건강관리에 대한 높아진 관심은 건강기능식품의 수요 성장을 견인하고 있다. 보건산업진흥원은 한국 식품산업 보고서에서 값비싼 의료비용이 건강기능식품 시장의 성장을 견인하는 배경으로 분석하고 있다[2].
식품의약품안전처에서 2017년 발표한 건강기능식품 생산실적 통계의 품목별 매출 현황에 따르면 홍삼과 비타민 및 무기질에 이어 프로바이오틱스(Probiotics)가 세번째로 높은 매출을 나타냈고 고시형 품목의 전체 매출액의 10.9%를 차지하였다[3]. 프로바이오틱스는 적당량 섭취 시 인체 내에서 유익한 활동을 하는 살아 있는 균으로 효모균, 박테리아 등을 통틀어 지칭한다. 대부분 유산균이며 Lactobacillus와 Bifidobacterium, Enterococcus 등의 균주가 포함된 제품이 발효유, 과립, 분말 등의 형태로 판매되고 있다. 장 내 미생물 조절에 따른 유해균 증식 억제 및 소화 개선 기능, 면역 강화기능성 등이 여러 연구를 통해 보고되면서 전 세계적으로 소비자들의 선택이 증가되고 있다[4]. 현재 프로바이오틱스는 의약품 및 건강기능식품으로 인허가 되어 판매되고 있으며, 최소한의 유산균 수가 함유된 의약품 유산균은 6세 미만의 급성 감염성 설사, 6 세 미만의 설사를 유발하는 항생제 치료에 따른 항생제 연관 설사, 그리고 괴사성 장염에 한하여 요양급여로 인정되어 투여되고 있다. 하지만 건강기능식품으로 판매되고 있는 생균 형태의 프로바이오틱스는 제품에 따라 1회분에 1 억에서 100억 마리까지 다량의 유산균을 함유하고 있다. 프로바이오틱스 유해 사례에 따르면 정상인에서도 복통, 설사, 복부팽만, 급성설사 등 이상반응이 보고되었지만 일시적이었다. 반면 신장이식 환자, 면역결핍질환자, 정맥 카테터, 혹은 심장 판막질환자 등에게 생균 투입은 감염의 원인이 되어 심장내막염이나 폐렴 등에 노출될 수 있고, 궤양성 대장염 등 염증성 장질환의 경우 균혈증에 따른 내장 기관으로의 박테리아 전이 및 패혈증 등 감염질환 유발이 제시되었다[5-7]. 특히 2018년 4월 50대 여성이 프로바이오틱스가 포함된 식품 섭취 후 패혈증으로 사망하는 사건이 발생해 논란이 되면서 안전성과 과잉복용에 대한 경각심이 확대되고 있다[8].
프로바이오틱스의 대표적인 유산균 Lactobacillus은 포도당을 발효하여 젖산(lactic acid)을 주로 생산하므로 장 내의 pH를 낮춰 알칼리성의 병원성 박테리아의 성장을 억제하는 효과가 있다. 하지만, 구강 내에서는 Lactobacillus가 전체 구강 내 세균총의 1% 미만임에도 불구하고 내산성으로 인해 법랑질을 침범한 우식 환부가 존재하면 이 곳에 다량으로 증식하면서 깊은 우식 진행에 관여한다. 특히 Lactobacillus는 생물막(biofilm)이라는 다당체를 생산하여 이를 매개로 인접 세균과 응집을 형성하여 생존에 불리한 환경에서도 지속적이고 충분한 개체군을 유지시키는 특성을 가지고 있기 때문에 Lactobacillus가 집락화 되는 것은 주변 환경을 보다 산성화 하여 우식 진행을 가속화할 수 있다[9]. 하지만 최근에는 프로바이오틱스를 이용하여 건강한 구강 내 환경을 조성하기 위한 많은 연구 결과들이 보고되고 있다. 특히, 프로바이오틱스가 치주질환 유발균의 집락화를 저해하는 면역 조절과 높은 관련성을 나타냈는데, 프로바이오틱스 균주가 우식균인 Streptococcus mutans의 생육 저해 효과를 나타냈으며, 치주질환 유발 균주들의 생육을 저해했으며 구취 유발 요인인 휘발성 황화합물 생성 균주의 생육을 저해했다[10,11].
이용의 편의성 때문에 분말형 프로바이오틱스는 높은 소비자 판매를 나타내고 있지만, 시판 제품에는 복용시기, 복용량, 그리고 복용법에 대한 구체적인 정보가 제조사에 의해서 제시되지 않고 있다. 대부분 ‘1회 1포씩 식후에 섭취하십시오’와 같은 간단한 복용법만 명기되어 있어 개인마다 복용시기나 복용법이 상이하다. 더욱이 부작용이 야기될 수 있는 전신상태 및 구강 상태가 고려된 주의사항은 대부분의 제품에서 제공되지 않고 있다[12]. 특히, 제품 중에는 혼합 유산균 분말 이외에도 말토오스나 말티톨과 같은 올리고당이나 무수결정포도당, 덱스트린, 식품향료 분말, 비타민 B 혼합제제, 비타민 C 등이 함유되어 있어, 단맛이나 청량감 등 기호성이 좋아져 물과 함께 복용하지 않는 경우가 많다. 소비자에게 부족하게 제공되는 제품 사용 정보로 인해 프로바이오틱스의 유익한 기능성에도 불구하고 제품 소비량 증가에 따른 부작용 사례 증가는 쉽게 예견해 볼 수 있다.
본 연구에서는 분말형 프로바이오틱스의 섭취 방법에 따라 변화되는 구강 환경을 관찰하고, 이를 통해 보다 적절한 프로바이오틱스의 복용 방법 및 복용 시 고려해야 할 주의사항을 알아보고자 하였다.
연구방법
1. 연구대상
전신질환이 없으며, 잔존치가 존재하는 20~30대의 건강한 성인 지원자를 대상으로 진행하였다. 그 중 틀니를 사용하지 않고, 교정치료 중이 아니며 최근 3개월 이내에 항생제, 소염제와 같은 구강 환경 변화를 유도할 수 있는 약을 복용하지 않는 대상자를 선정하였다[13]. 대상자 모집은 자체 제작 공고문을 통하여 사회관계망 서비스(SNS)와 E대학교 커뮤니티에 게시하여 모집하였다. 연구대상자 수는 G*power 3.1.9 program을 이용하여, 중간크기의 효과크기인 0.25, 유의수준 0.05, 80%의 검정력, 3그룹에서 5회 측정을 기준으로 F 분포를 사용하여 계산되었으며 최소 표본 크기는 96명으로 추산되었다. 본 연구에서는 탈락률을 고려해 지원자 중 총 110명을 선정하였다. 대면조사로 일반적 사항과 구강건강관리 설문을 실시하였고, 이 과정에서 항히스타민제를 복용 중인 1명이 제외되어 최종 109명의 자발적 실험 참가자가 본 연구의 분석대상이 되었다. 모든 참여자는 임상시험과 설문 시작에 앞서 연구의 목적과 취지에 대한 설명을 들었으며 연구 참여 동의서의 서명을 받았다. 본 연구는 00대학교 연구윤리심의위원회의 승인(IRB No. EUIRB2019-87)을 받고 진행되었다.
2. 연구방법
1) 연구설계
시험대상자는 무작위 할당을 통하여 총 3개의 군, 즉 대조군, 실험군 1, 실험군 2로 배정되었다. 프로바이오틱스는 판매량이 높은 J사 제품으로 통일하였다. 당류에 의한 연구 결과의 영향을 고려하여, 본 연구에는 합성착향료나 합성감미료 등이 첨가되지 않고 5종 균주(락추로스분말, 락토바실러스 아시도필루스(NCFM), 비피도박테리움 락티스, 락토바실러스 람노서스, 락토바실러스 아시도필루스(LA-14))가 함유된 제품을 선택하여 사용하였다. 대조군은 총 30명으로 분말형 프로바이오틱스를 섭취하지 않도록 하였고, 실험군 1은 40명이 배정되어 분말형 프로바이오틱스를 혀에 녹여서 섭취하도록 하였으며, 실험군 2는 39명을 대상으로 분말형 프로바이오틱스를 혀에 녹여 먹은 후 물로 헹구도록 하였다. 모든 대상자들은 실험 전에 칫솔과 혀클리너를 제공받았고 동일한 구강 환경에서 동시에 진행되었다. pH 값의 측정은 칫솔질, 혓솔질을 시행한 직 후 모든 군이 동시에 pH 시험지를 혀와 15초간 접촉하여 섭취 전의 pH 값을 측정한 것을 시작으로, 그 후 실험군 1과 실험군 2는 각각 해당하는 방법으로 프로바이오틱스를 섭취한 후 대조군을 포함하여 다시 한 번 동시에 pH 시험지를 접촉시켜 직후의 값이 측정되었다. pH 측정시기는 스테판 곡선에 근거하였고, 분말형 프로바이오틱스를 복용 후 삼키는데 소요되는 시간을 고려하여 3분 후 최초 측정되었고, 7분과 20분 후의 pH값 변화를 관찰하였다. 각 시험대상자마다 5개의 pH 값을 확보하였다.
2) pH 값의 수량화
연구대상자의 모든 pH 시험지는 동일한 장소, 동일한 연구자, 동일한 위치에서 FUJIFILM X-T20 모델(FUJIFILM body Black X-T20, Fujifilm Corporation, China)을 사용하여 촬영되었다. Photoshop 프로그램(Adobe creative cloud 2018, Adobe corporation, US)을 사용하여 동일한 연구자에 의해 흑백으로 전환 후, 명도 값을 사용하여 수치화하였다. 범위 내 색을 선택 시에 균등한 색을 얻기 위하여 촬영된 pH 시험지 두 지점의 pH를 가장 최소단위인 가로 세로 1픽셀로 변환한 후 픽셀의 명도를 확인하여 입력처리하였다.
3. 자료분석
연구 대상자의 일반적 특징으로는 성, 연령그룹(20~22, 23~26, 27세 이상), 흡연유형(흡연, 비흡연), 음주횟수(거의 먹지 않음, 가끔(주1~2회), 주 5회 이상), 주관적 구강건강(좋음, 나쁨), 스케일링 경험유무(예, 아니오)가 조사되었다. 이 중 주관적 구강건강은 중앙 응답의 편향을 막기위해 4점 척도로 조사되었고, 최종 분석 시에는 표본수를 고려하여 이분형화 하였다. 음주 횟수는 거의 먹지 않는 그룹, 가끔, 자주 먹는 그룹 정도를 구분하기 위한 것이었으며, 이를 포함한 일반적 사항에 관한 문항 모두 범주형 변수 형태로 질문되었다. 이들의 분포를 파악하기 위해 빈도와 백분율을 산출하였고 대조군과 실험군별로 인구집단의 특성을 살펴보았다. pH 농도의 정규성 여부를 보기 위해 Shapiro-Wilk normality 검정을 실시하였고, 그 결과 정규성을 만족하지 않아 Kruskal-Wallis 검정을 통해 그룹별 유의성을 살펴보았다. 이후 Tukey의 다중 비교법을 이용하여 사후검정을 실시하였다. 반복측정자료를 고려한 시간에 따른 경향성은 그룹의 평균과 신뢰구간이 나타난 그래프를 사용하여 비교하였다. 전체적인 제1종 오류 수준은 0.05로 적용하였고, R software version 3.5.1(R Development Core Team, Vienna, Austria)을 사용하였다.
연구결과
1. 일반적 특성과 군별 인구학적 분포
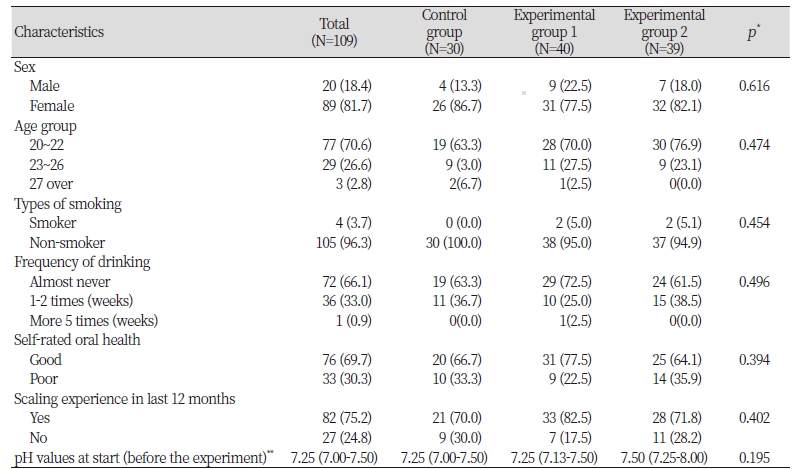
총 109명의 연구대상자 중 여성이 89명으로 81.7%를 차지하였고 연령 세 그룹 중 20대 초반(20~22세)이 70.6%로 가장 높게 나타났다. 흡연 유형으로는 비흡연자가 96.3%로 대부분을 차지하였으며, 음주 횟수로는 ‘거의 먹지 않음’이 약 66%, ‘가끔(주 1~2회)’이 33%를 차지했다. 주관적 구강건강은 ‘좋음’이 76명(69.7%), ‘나쁨’이 33명(30.3%)으로 나타났고 지난 12개월 내의 스케일링 경험 유무에 관해서는 약 75%가 ‘경험 있다’고 응답하였다. 대조군과 실험군별로 배정된 연구대상자의 일반적 특성에 따른 분포를 비교한 결과, 모든 변수에서 유의한 차이 없이 고르게 분포되었다. 실험 시작 시 pH 값의 중앙값(median value)과 사분위수 범위(interquartile range, IQR) 또한 각 실험군별로 유의한 차이가 없었다(chi-squaared value=3.271, p-value=0.195)<Table 1>.
2. 시간대별 pH 변화
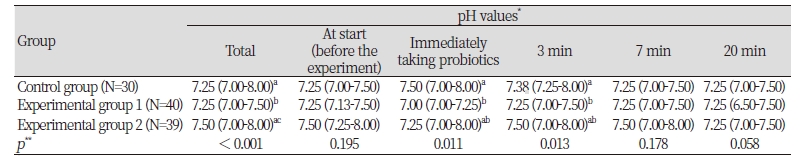
5번의 pH 측정 값을 모두 합친 전체적인 pH 값은 실험군 2(먹은 후 물로 헹구는 군)에서 가장 높았고, 실험군 1(혀에 녹여 먹는 군)과 대조군에서는 유사한 중앙값(대표값)을 보였으나 산포도를 고려하였을 때는 실험군 1에서 가장 낮은 pH 값을 보였다. 군별 통계적 유의성은 실험군 1과 대조군(p<0.001), 실험군 1과 실험군 2에서 유의한 차이를 보였다(p<0.001)<Table 2>. 실험 시작 시의 pH 값을 포함하여 분말형 프로바이오틱스 섭취 직후, 3분 후, 7분 후, 20분 후 각각에서의 pH 값의 분포에서는 섭취 직후와 섭취 3분 후에서 군별로 유의한 차이가 있었다. 사후검정결과 두 시간대 모두 대조군과 실험군 1에서 집단간 차이를 발견하였다<Table 2>.
3. 군별 시간경향성(time trend)
반복 측정된 pH 값의 시간에 따른 경향성을 군별로 살펴보았다. 대조군에서는 pH 값이 시간에 따라 증가하였다가 감소한 후 다시 회복되는 형태를 보였고, 실험군1(혀에 녹여 먹는 군)과 실험군2(먹은 후 물로 헹구는 군)는 전반적으로 유사한 패턴을 보였다. 그러나 프로바이오틱스 복용직 후의 pH변화를 살펴보면, 실험군 1에 비해 물과 함께 복용하는 실험군 2에서의 변화가 더 작은 것으로 나타났다. 프로바이오틱스를 물과 함께 복용하거나 물 없이 복용하여도 섭취 후 5분 정도 후에는 실험 전 측정된 타액의 pH와 유사한 값을 보였다<Fig. 1>.
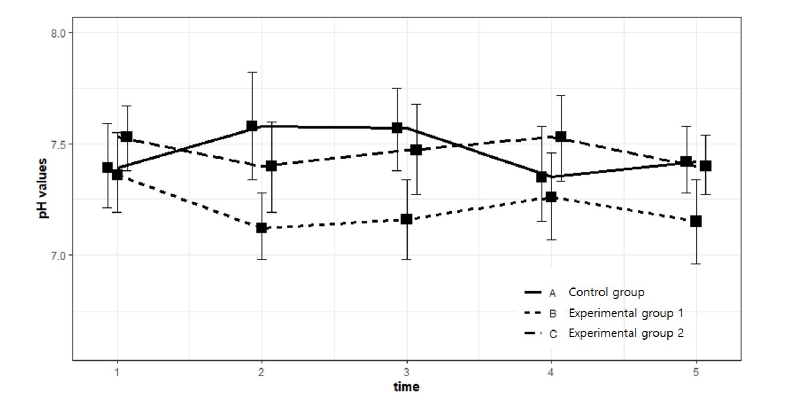
Fig. 1. The plot of time trend of pH values according to 5 time points (at start, Immediately after taking probiotics, 3 min, 7 min and 20 min) with groupwise means and confidence intervals considering repeated measurement data. Solid line stands for control group (A), dotted line stands for experimental group 1 (B), and longdash stands for experimental group 2 (C).
총괄 및 고안
본 연구에서는 최근 판매율이 급증하고 있는 프로바이오틱스의 복용 방법에 따른 구강 환경 변화를 관찰하였고 이를 바탕으로 프로바이오틱스 복용 시 유의 되어야 할 사항을 도출하였다. 식품의약품안전처가 기능성을 인정한 프로바이오틱스 균주는 19종으로, Lactobacillus 11종, Bifidus(Bifidobacterium) 4종, Lactococus 1종, Enterococcus 2종, Streptococcus 1종 등이다. 장내 유해균 증식 억제, 변비 및 설사 개선, 급성 감염성 설사 및 항생제 복용 후 설사 개선, 면역세포 기능 활성화, 유당 불내증 개선 효과 등이 보고되면서 소비자들의 선택이 증가되고 있다[14]. 이와 더불어 구강 질환에 대한 프로바이오틱스의 작용에 관한 연구들도 꾸준히 진행되고 있다.
Lactobacillus reuteri를 투여한 경우 치은염 환자의 프라그 형성과 잇몸 염증이 줄어들고 치은열구의 혈청(crevicular fluid) 양과 염증성 사이토카인 interleukin 8(IL-8)과 tumor necrosis factor alpha(TNF-α) 및 출혈이 크게 감소된 것으로 조사되었다. 치주질환자에게는 치은염 평가지수(gingival index)와 세균 프라그의 양이 감소되었으며, 치주질환 원인균인 Porphyromonas gingivalis와 Prevotella intermedia의 증식을 각각 82%, 65% 억제하는 것으로 조사되어, 프로바이오틱스 투여가 구강 내 정상세균 수립에 효과적임이 제시되었다[15,16]. Weissella cibaria 균이나 Streptococcus salivarius 균의 투여는 Fusobacterium nucleatum 같은 구취 원인균의 휘발성 황화합물(Volatile sulfur compounds; VOCs) 생성을 감소시키고[17], Lactobacillus rhamnosus 균은 Porphyromonas gingivalis와 F. nucleatum의 VOCs를 감소시키는 것으로 보고되었다[18]. Lactobacillus로 발효시킨 우유를 장기간 섭취한 경우 충치 원인균인 Streptococcus mutans의 생육 억제가 관찰되었다[19]. Lactobacilli는 우식증 테스트에 적용될 만큼 충치와 밀접하게 인식되어 왔지만, 일부 Lactobacillus의 경우 연쇄상 구균성 병원체에 의한 치아 우식을 억제하는 것으로 조사되어, 구강 건강에서 프로바이오틱스로 작용할 수 있는 유익한 일부 Lactobacillus에 대한 관심도 증가되었다[20].
그럼에도 불구하고, 프로바이오틱스 제품이 건강한 모든 성인에게 일관된 건강 기능성을 나타내지 않았고[21], 프로바이오틱스에 포함되는 균주들의 항생제 저항성, 대사성 및 용혈성 활성, 독소 생산, 면역력 억제, 감염력 등의 우려에 따른 부작용 조사 필요성을 세계보건기구(WHO)와 국제연합식량농업기구(FAO)에서는 권고하고 있다. 프로바이오틱스의 소비 증가와 함께 부작용도 함께 증가되어, 주로 소화기 및 장기 통증, 두드러기 등의 위해사례가 한국소비자원에 신고되고 있다. 특히, 프로바이오틱스 제품 중에는 혼합 유산균 외에도 올리고당이나 무수결정포도당과 같은 다양한 당류가 함유되어 있으므로 구강 내에 잔존이 지속된다면 오히려 뮤탄스균 등에 의한 치아우식 위험을 증가시킬 수 있다. 본 연구에서는 구강으로 복용되는 분말 형태의 프로바이오틱스 성분이 복용 방법에 따라 타액의 수소이온농도(pH)에 미치는 영향을 관찰하였다. 실험 결과, 프로바이오틱스를 물과 함께 복용하거나 물 없이 복용하여도 섭취 후 5분 정도에는 실험 전 측정된 타액의 pH와 유사한 값을 나타냈다. 하지만, 물과 함께 프로바이오틱스를 복용한 이후의 pH 변화와 비교하여 물 없이 복용한 이후의 pH 감소가 더 큰 것으로 관찰되었으며, 이는 통계적으로 근사적 유의성을 보였다(Tukey 사후 검정통계량(실험군 1과 실험군 2), 섭취 직후, t=1.959, p=0.127; 3분 후 t=2.276, p=0.064). 반복적이고 장기적인 복용을 고려했을 때 분말 형태의 프로바이오틱스는 물과 함께 복용하는 것이 pH 감소에 따른 치아우식증이나 구강 질환 예방에 도움이 될 것으로 판단된다. 프로바이오틱스는 위산에 의해 변성되어 생균으로서의 역할을 기대할 수 없으므로 공복이나 식후 30분 이후 복용이 일반적으로 권장되고 있다. 프로바이오틱스 제품의 사용 목적이 구강 조직과 직접적인 접촉을 요구하는 경우가 아니라면 물과 함께 복용되는 캡슐 형태의 제품이 구강 내 수소이온농도 변화에 따른 치아 우식이나 구강 질환 위험성 감소에 도움이 될 것으로 생각된다. 또한 프로바이오틱스 제품에 혼용되어 있는 다양한 당류도 치아 우식 위험성을 높이므로 물과 함께 복용하는 것이 권장할 수 있는 프로바이오틱스 제품 복용법이라 사료된다.
프로바이오틱스는 다양한 균주들로 구성되어 있으므로 개인마다 나타날 수 있는 유해성은 다를 것으로 예상된다. 과거 유산균에 들어갔던 Enterococcus 균이 항생제 내성을 유발하는 것으로 밝혀져 프로바이오틱스 제품 사용이 금지되는 일례도 있다[22]. 프로바이오틱스 복용 전에는 각 개인이 가지고 있는 전신과 구강의 만성질환이나 염증성 질환 그리고 알러지 등을 전문가와 상담하는 것이 필요하며 이는 부작용을 최소화하며 프로바이오틱스의 유효성을 얻을 수 있는 방법으로 사료된다. 또한 본 연구 결과에서 제시한 바와 같이 분말 형태의 프로바이오틱스는 생균임을 인지하고 구강 내 잔존 시간에 따른 부작용을 고려하여 물과 함께 복용하게 하는 소비자들의 섭취 형태 변화 유도가 필요하다. 다만, 본 연구는 프로바이오틱스 복용 후 단 시간에 발생하는 구강 내 pH 값의 변화를 측정한 결과를 근거로 하여 복용 방법을 제시하고 있기 때문에, 보다 정확한 근거를 통한 복용 방법을 제시하기 위해서는 장기적인 복용 후 구강 환경 변화를 관찰하는 후속 연구가 필요할 것으로 사료된다. 제품 판매사 또한 분말형 프로바이오틱스의 적절한 복용 방법 및 고려되어야 할 주의사항에 대한 보다 자세한 정보를 소비자에게 제공해야 될 것으로 판단된다.
결론
본 연구에서는 소비자의 이용이 급증하고 있는 분말형 프로바이오틱스의 섭취 방법에 따른 구강 내 환경변화를 알아보고자 시행되었다. 연구결과, 분말형 프로바이오틱스는 물과 함께 복용하는 방법이 구강 내 pH 변화를 감소시키는데 도움이 되는 것으로 나타났다. 프로바이오틱스는 생균임을 인지하고 구강 내 잔존 시간에 따른 부작용을 고려하여 적절한 복용 방법 및 주의사항에 대한 보다 자세한 정보가 소비자에게 제공되어야 한다. 이 연구는 프로바이오틱스 복용의 표준화된 섭취방법 권고안을 마련함에 있어 본 연구 결과가 하나의 근거자료로 사용되길 기대한다.