서 론
우리나라 영구치 우식증은 20세 무렵에 이르면 90% 이상 대다수의 국민들이 경험하고 있고, 특히 저소득계층이나 장애아동은 치과의료 이용의 어려움으로 치아우식 발생이 상대적으로 높은 것으로 보고되고 있다[1].
치아우식증은 구강 내 세균에 의해 생성된 산에 의해서 수산화인회석(Ca10(PO4)6(OH)2)으로 이루어진 법랑질 결정이 용해되는 것으로, 초기에 탄산이온과 마그네슘을 먼저 용해시키고, 좀 더 용해가 어려운 칼슘과 인산 등 이온을 차례로 용해시킨다[2,3]. Voegel과 Frank [4]는 산에 의한 법랑질 용해는 법랑질 결정의 끝부분 중앙에서 부터 내부 방향을 따라 진행 하고, 중앙부 파괴 이후 측방부의 파괴로 확장한다고 하였다. 선행 연구들은 산 생성 세균 등이 치아의 표면에는 최소한의 손상을 주지만, 미세공극을 통하여 표면 하방을 탈회시키는 치아우식의 초기 단계 개념을 입증하였다[5,6].
이런 치아우식 초기에는 타액 내의 칼슘이나 인, 불소 등 예방적 처치를 통해 법랑질의 재광화가 가능하다고 할 수 있다[3]. 치아우식 예방과 초기우식법랑질 재광화에 효과가 있는 것으로 알려진 제재들[7-9] 중 죽염은 소화제와 해독제, 염증치료 등에 사용되어져 왔다[10]. 죽염은 대나무 탄화 시 많은 미네랄이 잔류하며 굽는 횟수가 거듭될수록 Ca과 K의 함량이 증가하고, 이밖에도 Fe, Mg 등의 천연 미네랄을 함유하고 있다고 보고하였다[11,12].
이러한 죽염은 치은의 염증 완화에 효과가 있다고 보고되었고[8], 치아우식 재광화에 대한 연구에서 홍 등[13]은 불화나트륨에, 김 등[14]은 일불소인산나트륨에 죽염을 배합한 치약 처치 시 법랑질 표면의 경도가 증가하고 불소 침착 효과가 높게 나타났다고 보고하였다. 최 등[15]은 초기우식법랑질에 불화나트륨과 죽염이 배합된 치약 처리 시 표면 하방의 병소의 깊이와 무기질 손실량이 감소되었다고 하였고, 오 등[16]은 3% 죽염 용액을 우식법랑질에 처리한 후 법랑질 표면 하방의 밀도가 증가되었다고 보고하였다. 이와 같이 초기우식법랑질이 형성된 부위에 재광화가 이루어진다면 표면하방 병소의 무기질 밀도가 증가하고 경도 또한 증가할 것으로 사료된다. 하지만 국내에서 죽염의 치아우식증 예방 효과를 평가한 연구들은 대부분 표면의 경도를 측정하거나 미세전산화단층촬영술 등을 이용하여 표면하방의 병소깊이나 밀도를 평가하였고, 법랑질 표면 하방의 병소 깊이에 따른 경도를 평가한 연구는 이루어지지 않은 실정으로 표면 하방의 경도를 측정해 볼 필요가 있다고 사료되었다.
따라서 본 연구에서는 법랑질 표면 하방의 병소 깊이에 따른 재광화 효과를 평가하고자 인공적으로 초기우식을 형성한 소 치아에 죽염, 불화나트륨, 그리고 죽염과 불화나트륨이 혼합된 용액을 적용한 후 법랑질 표면하방 80 µm 깊이까지의 경도를 측정하여 죽염이 표면하방의 경도를 증가시키는지를 평가하고자 하였다.
연구방법
1. 연구재료 및 방법
1) 시편제작 및 실험용액
본 연구에서 시편제작은 건전한 소의 영구 절치를 시편절단기(IsoMet® low speed saw, Buehler, Illinois, USA)를 이용하여 백악법랑경계부에서 수평으로 절단한 후 설면결절 부위를 수직으로 절단하였다. 절단된 시편의 순면을 제외하고 나머지 부위는 네일바니쉬를 도포하고 4시간 동안 건조 시킨 후 재 도포하여 사용하였다. 사용된 시편은 군 당 4개씩 총 12개 시편을 사용하였다.
본 연구에서 실험용액은 3% 죽염[16,17] (bamboo salt, Kaeam, Seoul, Korea, 이하 BS)과 2% 불화나트륨[18] (sodium fluoride, Sigma, Saint Louis, USA, 이하 NaF) 그리고 죽염과 불화나트륨의 혼합에 따른 효과를 비교하기 위하여 3% BS와 2% NaF를 혼합한 용액을 사용하였다. 각 실험용액은 BS군은 3차 증류수 100 mℓ에 죽염 3 gm을 넣고, NaF군은 100 mℓ에 NaF 2 gm을 넣어 5분 동안 교반하여 용해시켰으며, BS와 NaF를 혼합한 군은 먼저 3차 증류수 100 mℓ에 NaF 2 gm을 넣어 5분 동안 교반하며 용해시킨 후 죽염 3 gm을 넣고 5분 동안 교반하며 용해시켜 제조하였다.
2) 초기우식법랑질 형성 및 재광 화용액 처리
초기우식법랑질 형성을 위해 정상 법랑질 시편을 오 등[16]의 연구와 동일하게 수산화인산칼슘(calcium phosphate tribasic, Sigma, USA)이 50% 포화된 0.1 M의 젖산과 0.2% Carbopol ETD 2050 (Lot. #EC 464CD758, Noveon, Inc. Cleveland, OH, USA)을 첨가한 후 50% NaOH를 첨가하여 용액의 최종 pH를 5.0으로 조절하여 제조된 탈회용액 15 mℓ에 시편을 1개씩 침지시켜 37°C 배양기에서 72시간 동안 처리하였다. 탈회용액 처리 후 초기우식부위를 보존하기 위하여 시편의 순면 1/2 부위에 네일바니쉬를 도포하였다. 그 후 제조된 재광화 용액 10 mℓ에 시편을 1개씩 침지시킨 후 37°C 배양기에서 200 rpm으로 교반하면서 24시간 동안 처리하였다[16,18]. 재광화 용액 처리 후 시편 표면을 흐르는 증류수에 1분 동안 세척하여 습윤 상태로 보관하였다.
3) 표면미세경도측정기 및 주사전자현미경을 이용한 법랑질 표면하방 관찰
재광화 용액 처리 후 분석을 위하여 시편은 네일바니쉬가 도포된 초기우식법랑질 부위와 재광화 부위가 포함되도록 절단연에서 치경부 방향으로 절단하였다. 절단된 시편의 한쪽면은 표면하방의 법랑질 결정 양상을 평가하기 위하여 주사전자현미경(scanning electron microscope, Hitachi, S-4700, Tokyo, Japan, 이하 SEM)을 이용하여 측정하였고, 다른 쪽 절단면은 법랑질 표면하방을 표면미세경도측정기(Fm-7, Future-tech Corp, Tokyo, Japan)를 사용하여 미세경도(vickers hardness number, 이하 VHN)를 측정하였다.
먼저, 절단된 한쪽면은 SEM 분석을 위하여 관찰할 절단면은 손상시키지 않으며, 시편의 두께가 3 mm 이내가 되도록 제작하였다. 그 후 시편을 48시간 동안 탈수시켜 백금으로 코팅하여 15 kV 가속전압 하에서 SEM 분석을 실시하였다. 관찰은 1,000배 배율로 하였다.
다른 쪽 절단면은 VHN 측정을 위하여 직경 3cm의 고무 틀에 측정될 절단면이 위쪽을 향하도록 위치시킨 후 자가중합형 레진으로 포매하고 연마지(Carbimet, Buehler, Illinois, USA) #60, #240, #600, #1,200번을 사용하여 순차적으로 연마 하였다. VHN 측정은 시편 표면의 변형 가능성을 고려하여 시편의 표면에서 부터 5 µm 떨어진 부위를 시작 부위로 지정하고, 10 µm, 20 µm, 30 µm, 50 µm, 80 µm 깊이의 위치에서 측정하였다. 측정은 표면경도계를 이용하여 200 gm의 하중으로 10초 동안 압인[15]하였고, 한 시편 당 편차를 줄이기 위하여 각각의 깊이에서 좌, 우, 중앙 3부위를 측정하여 VHN 평균값을 사용하였다.
2. 자료 분석
초기우식법랑질 부위와 재광화 부위의 표면하방의 VHN을 측정한 후 표면하방 5 µm, 10 µm, 20 µm, 30 µm, 50 µm, 80 µm 깊이에서의 평균과 표준편차를 산출하였으며, 재광화 용액 처리 전과 후의 VHN 변화를 살펴보기 위하여 정규성 검정 후 one-way ANOVA를 시행하였다. 사후검정 방법으로 Tukey test를 사용하였다. 모든 통계는 SPSS 21.0 (SPSS Inc., Chicago, IL, USA) 프로그램을 이용하여 분석하였으며, 통계적 유의성 판정을 위한 유의수준은 5%로 고려하였다.
연구결과
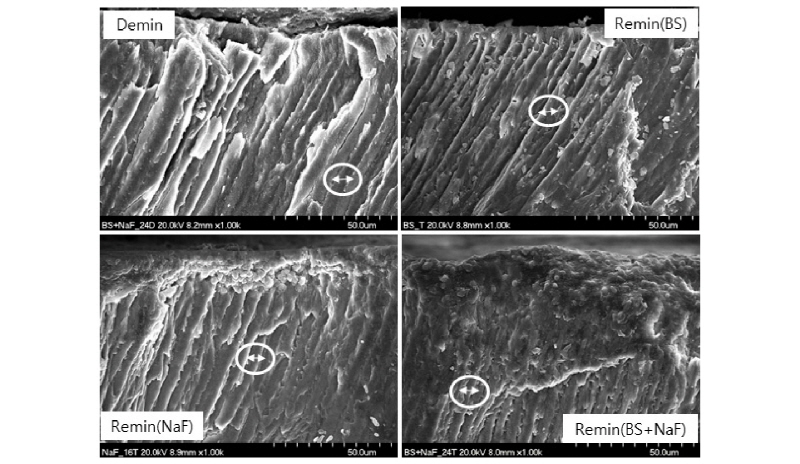
1. SEM을 이용한 초기우식법랑질 표면하방의 양상
SEM을 이용하여 표면 하방을 관찰한 결과 초기우식법랑질 표면하방의 법랑질 결정들이 탈회로 인해 격자 간격이 넓어진 양상을 보였다. 재광화 용액 처리 후 BS군은 법랑질 표면 하방 결정들이 표면부터 하방으로 일정한 방향으로 배열되어 있었으며, 초기우식법랑질 부위의 결정보다 격자 간격이 약간 좁아진 양상을 보였다. NaF군은 법랑질 표면 하방 20 µm 깊이 정도까지 구형의 결정들이 보였고, 20 µm 깊이 하방부터 배열되어 있는 법랑질 결정의 격자 간격이 초기우식법랑질 부위의 결정보다 좁아진 양상을 보였다. BS+NaF군은 법랑질 표면 하방 30 µm 깊이 정도까지 형성된 구형의 결정들이 NaF군 보다 작고 조밀한 형태를 보였고, 30 µm 깊이 하방부터 배열되어 있는 법랑질 결정의 격자 간격이 초기우식법랑질 부위의 결정보다 좁아지고 결정 사이의 미세공극이 메워져 있는 양상을 보였다<Fig. 1>.
2. 초기우식법랑질 및 재광화 부위 표면하방 미세경도 평가
1) 초기우식법랑질 표면하방 미세경도 평가
초기우식법랑질 부위의 표면하방 80 µm 깊이까지의 경도측정 결과 총 VHN 값이 BS군 178.06, NaF군 193.30 그리고 BS+NaF군 191.97로 통계적으로 차이가 없었으나, 깊이별 경도 값 중 20 µm 깊이에서는 NaF군이 209.70으로 가장 높았으며, BS+NaF군 204.85 그리고 BS군 189.31 순으로 통계적으로 유의한 차이를 보이며 낮아졌다(p<0.05)<Table 1>.
|
Table 1. The VHN values according to depths of demineralized enamel subsurface Unit: VHN (Mean±SD) 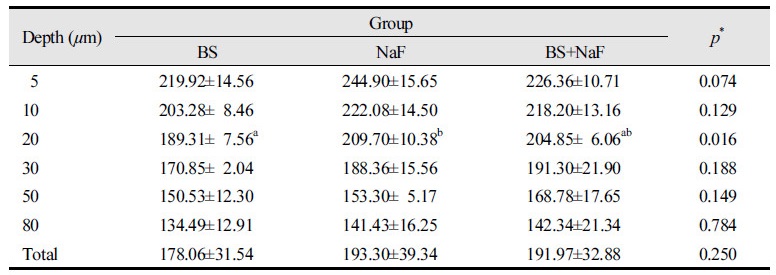
|
|
|
*by one-way ANOVA a,bThe same letter indicates no significant difference by Tukey test at ɑ=0 |
|
2) 재광화 부위 표면하방 미세경도값 평가
재광화된 법랑질 부위의 표면하방 80 µm 깊이까지의 경도 측정 결과 총 VHN 합계는 BS+NaF군 214.13로 가장 높았으며 NaF군 212.16 그리고 BS군 189.63 순이었다. 군간 깊이에 따른 경도 값을 살펴보면, 먼저 표면층에 가까운 5 µm 깊이에서는 NaF군이 272.77로 다른 두 군에 비하여 통계적으로 유의하게 높은 값을 보였으며(p<0.01), 20 µm와 30 µm 깊이에서는 NaF군이 각각 227.64와 226.75 그리고 BS+NaF군이 각각 208.65와 211.94로 BS군에 비하여 통계적으로 유의하게 높은 값을 보였다(p<0.01). 또한, 50 µm 깊이에서는 BS+NaF군이 202.84로 NaF군 173.99와 BS군 169.21보다 통계적으로 유의하게 높은 값을 보였으며(p<0.01), 80 µm 깊이에서도 BS+NaF군이 160.40으로 통계적인 차이는 없지만 다른 두 군에 비하여 높은 값을 보였다(p>0.05)<Table 2>.
|
Table 2. The VHN values according to depths of remineralized enamel subsurface Unit: VHN (Mean±SD) 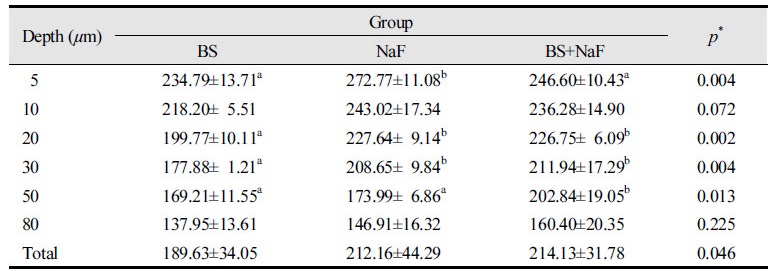
|
|
|
*by one-way ANOVA a,bThe same letter indicates no significant difference by Tukey test at ɑ=0 |
|
3) 재광화 용액 처리 전․후 표면하방 미세경도 변화도 값 비교
재광화 용액 처리 후 초기우식법랑질 부위와 재광화된 법랑질 부위의 표면하방 80 µm 깊이까지의 변화된 경도값의 총 합계는 BS+NaF군이 22.16, NaF군이 18.87로 BS군의 11.57 보다 통계적으로 유의하게 많은 증가량을 보였다(p<0.001). 군간 깊이에 따른 변화된 경도값을 살펴보면, 5 µm 깊이에서는 NaF군이 27.87로 다른 두 군에 비하여 통계적으로 유의하게 증가된 값을 보였으며(p<0.01), 20 µm와 30 µm 깊이에서는 NaF군이 각각 17.94와 20.30 그리고 BS+NaF군이 각각 21.90과 20.63으로 BS군의 10.46과 7.03에 비하여 통계적으로 유의하게 증가된 값을 보였다(p<0.01, p<0.05 ). 또한, 50 µm와 80 µm 깊이에서는 BS+NaF군이 각각 34.06과 18.06의 증가량을 보이며, NaF군의 20.69와 5.49 그리고 BS군의 18.68과 3.46의 증가량 보다 통계적으로 유의하게 높았다(p<0.001)<Table 3>.
총괄 및 고안
치아에서 탈회는 구강 내의 세균에 의해 생성된 유기산이 법랑질의 미세공극을 통해 확산되어 법랑질의 내부를 용해시키고 다시 용해된 광물이 법랑질 표층부에 침전을 일으키는 복잡한 현상이라고 하였다[19]. Anderson [20]은 법랑질 초기 우식은 구강내 환경에 따라 탈회가 중단되거나 재광화 될 수 있음을 보고하였다.
현재까지 잘 알려진 재광화 물질인 불화나트륨은 안정성이 높아, 전문가 불소도포나 자가 불소양치 용액으로 사용되고 있다[21]. 또한, 불소 이외에 재광화에 효과가 있는 것으로는 카제인 포스포펩타이드 무정형 인산칼슘(casein phosphopeptide amorphous calcium phosphate, 이하 CPP-ACP) [9], 수산화인회석이 배합된 치약[7], 죽염[8,15] 등이 있다. 이 중 죽염은 대부분 법랑질 표면의 경도 변화[8,13]와 표면 하방의 밀도 변화[15-17] 등을 평가하여 재광화 효과를 보고하였는데, 법랑질 표면하방의 깊이에 따른 경도를 측정하여 재광화 효과를 평가하는 것이 필요하다고 사료되었다. 따라서 본 연구에서는 죽염, 불화나트륨 그리고 죽염과 불화나트륨을 혼합한 용액을 재광화 용액으로 선정하여 처리한 후 법랑질 표면하방의 법랑질 결정 양상과 경도 변화를 평가하였다.
본 연구에서 죽염은 기존 연구[15-17]들을 토대로 3% 농도로 사용하였고, 불화나트륨은 Duschner 등[18]이 인공우식 법랑질에 24시간 동안 2% 불화나트륨을 도포한 후 법랑질 표면과 하방부위 양상을 관찰한 결과 재광화 양상을 관찰할 수 있었다고 보고한 것을 바탕으로 2% 불화나트륨 용액을 선정하여 24시간 동안 시편에 처리하였다.
본 연구에서 시편 처리 후 법랑질 표면하방의 결정 양상을 SEM으로 관찰한 결과 인공적인 탈회로 초기우식법랑질이 형성된 부위는 표면하방의 법랑질 결정들의 격자 간격이 넓어진 양상으로 배열되어 있었다. 그리고 재광화 후 BS군은 표면하방의 법랑질 결정들의 간격이 탈회 부위보다 약간 좁아진 양상으로 배열되어 있는 것을 확인할 수 있었다. Oh 등[22]이 3% 죽염 용액을 초기우식법랑질이 형성된 부위에 처리한 후 XRD 분석을 한 결과 법랑질 결정의 격자간격이 더 좁아져 결정성이 좋아졌다고 보고한 것과 같은 유사하였다. 본 연구에서도 죽염만 처리한 경우도 법랑질 표면 하방에서 미미하지만 격자 간격이 좁아져 법랑질의 재광화가 이루어진 것으로 보인다. 그리고 NaF군은 법랑질 표면 하방 약 20 µm 깊이까지 구형의 결정들이 형성되어있고, 그 깊이 하방부터 일정한 방향으로 배열된 법랑질 격자들의 간격이 좁아진 양상을 보였다. BS+NaF군도 법랑질 표면 하방 약 30 µm 깊이까지 구형의 결정들이 NaF군 보다 크기가 작고 조밀한 형태로 형성되어있는 양상을 보였고, 그 깊이 하방부터 일정한 방향으로 배열된 법랑질 결정들의 간격이 좁아졌고, NaF 군보다 미세공극이 메워져 있는 양상을 보였다. 법랑질 표면층에 형된 구형의 결정들은 김 등[14]이 죽염과 일불소인산나트륨을 배합한 치약을 처리한 후 법랑질 표면에 수산화인회석 구조와 같은 입자들이 무수히 많이 부착되어 있었다고 보고한 연구와 유사하게 표면층에 구형의 입자들이 형성된 것을 확인할 수 있었다. McCann과 Bullock [23]은 100 ppm 이하의 중성불화나트륨 용액은 불화인회석을 형성하고, 고농도 불소는 불화칼슘을 형성한다고 하였고, Joost-Larsen과 Fejerskov [24]는 NaF는 2%로 약 9,000 ppm의 불소를 사용하여 국소도포하기 때문에 주로 불화칼슘을 형성하게 된다고 보고하였다. 이러한 선행 연구들처럼 본 연구에서 법랑질 표면부터 20~30 µm 깊이 부위에 형성된 구형의 입자들은 2% NaF를 처리하여 형성된 불화칼슘인 것으로 사료된다. 불소가 수산화인회석과 결합하여 불화인회석을 이루면 매우 단단한 결합이지만 표면에 흡착되는 불화칼슘은 느슨한 불화물 결합으로[25] 타액에 의해 쉽게 용해될 수 있다. 그래도 ten Cate [26]는 불화칼슘은 구강 내에서 인산 또는 단백질로 코팅된 구형으로 존재하기 때문에 느리게 용해되고, 불소 저장고로서 재광화를 촉진시키는 역할을 한다고 하였다. 본 연구에서 BS+NaF군에 형성된 구형의 결정들은 NaF군 보다 조밀하며 조금더 크기가 작은 형태를 보였다. 이는 표면에 불화칼슘 이외에도 김 등[27]이 NaCl의 구조를 SEM을 이용하여 관찰한 결과 표면이 용융되어 매끄러운 포도송이 형태를 이루고 있음이 관찰되었다고 보고하였는데, 죽염 속의 다양한 무기질 성분들이 침착되어 불화칼슘과 함께 조밀한 형태로 형성된 것으로 사료된다. 본 연구에서는 BS+NaF군에서 표면 하방의 법랑질 결정 사이의 공극 부위가 미세한 입자들로 메꾸어져 있는 양상을 보였는데, 이러한 결과는 죽염과 불소의 상호작용과 죽염에 포함된 Ca, K, Na, Fe, Mg 등[11,12] 다양한 무기질 성분들의 영향인 것으로 사료된다.
본 연구에서 표면미세경도측정기를 이용하여 법랑질 표면하방의 경도를 측정한 결과 초기우식법랑질 부위의 경도 값은 3군간 차이가 없었지만 불소가 함유된 군의 값이 미미하게 높았으며, 20 µm 깊이에서는 NaF 군이 209.70으로 가장 높았다. 이러한 결과는 동일 시편에서 재광화 용액 처리 전과 후의 변화를 평가해 보고자 탈회된 부위를 네일바니쉬를 도포한 후 재광화 용액을 처리하였지만, 시편의 처리 동안 표면하방의 법랑질 결정들 사이의 미세한 공극을 통하여 재광화 용액이 탈회부위에 영향을 준 것으로 사료된다.
재광화 용액 처리 후 탈회된 법랑질 부위와 재광화된 법랑질 부위의 경도의 변화를 살펴보면 표면하방 80 µm 깊이까지에서 BS+NaF군은 22.16, NaF군은 18.87 그리고 BS군은 11.57씩 증가한 결과를 보였으며, 통계적으로 BS+NaF군과 NaF군이 BS군보다 유의하게 증가하였다. 본 연구에서 죽염만을 처리한 경우에도 미미하지만 경도의 증가를 보여 표면하방에서 재광화 효과가 있는 것으로 평가되었다. 이러한 결과는 오 등[16,17]이 3% 죽염 용액에 초기우식병소가 형성된 소 치아를 24시간 동안 침지한 경우와 14일 동안 처리한 경우 표면하방의 밀도의 증가량이 적기는 하지만 재광화 효과가 있었다고 보고한 것과 유사하다. 이는 죽염은 무기질 성분들이 다량 또는 미량으로 존재한다고 보고[12]한 것과 같이, 다양한 무기질들이 표면하방의 미세공극으로 침투하여 나타난 결과로 사료된다. 그리고 군간 깊이에 따른 경도의 변화는 5 µm 깊이에서는 NaF군이 27.87로 다른 두 군에 비하여 통계적으로 유의하게 증가되었지만, 50 µm와 80 µm 깊이에서는 BS+NaF군이 각각 34.06과 18.06으로 NaF군과 BS군의 경도 증가량 보다 통계적으로 유의하게 많이 증가한 결과를 보이며 표면층의 재광화 효과는 NaF군이 높았지만, 표면 하방 30 µm 깊이에서부터 80 µm 깊이까지에서 BS+NaF군의 재광화 효과가 높은 것을 확인할 수 있었다. 하 등[28]이 초기우식병소가 형성된 소 치아에 3% 죽염과 2% NaF를 혼합한 용액을 24시간 처리한 후 표면하방 100 µm 깊이까지의 성분을 분석 결과 NaF만을 처리한 군보다 F 성분이 통계적으로 유의하게 높았다고 보고한 것과 같이, 본 연구에서 불소가 죽염 속에 포함된 Ca, Mg 등과의 결합으로 우식 법랑질 표면 하방까지 깊이 침투했을 것으로 사료된다.
본 연구의 제한점은 동일한 실험조건이라 하여도 같은 치아 내에서도 약간씩 차이가 나타나기 때문에 표본간의 차이를 줄이기 위한 과정이 필요하리라 생각된다. 따라서 추후 이러한 문제를 해결하기 위해서는 탈회 후 법랑질 표면의 미세경도를 측정하여 VHN 값이 유사한 시편을 대상으로 실험을 진행하는 것이 필요하겠다. 또한, 본 연구에서는 시편을 4개로 시행하였지만 시편의 수를 증가시켜 편차를 줄이는 것도 필요하리라 생각된다. 마지막으로 본 연구에서는 in vitro로 연구로 죽염의 재광화 효과를 평가하였지만, 향후에는 실제 타액의 성분이나 구강미생물 등 여러 구강 내 환경 요인을 고려한 임상실험 연구가 필요하다고 사료된다.
이러한 연구의 한계에도 불구하고 본 연구결과는 초기우식법랑질 표면 하방의 깊이에 따른 경도를 평가함으로써 죽염과 불소를 혼합하여 사용한 경우 법랑질 표면 하방에서의 재광화 효과가 있음을 평가했다는 것에 의의가 있다고 사료된다.
결 론
본 연구는 초기우식병소를 형성한 소 영구 절치 시편에 3% 죽염, 2% 불화나트륨, 그리고 3% 죽염과 2% 불화나트륨을 혼합한 용액을 24시간 동안 처리한 후 시편 표면하방의 법랑질 결정 양상과 경도 변화를 SEM과 표면미세경도측정기를 이용하여 분석하고 다음과 같은 결과를 얻었다.
1.SEM을 이용한 법랑질 표면하방의 결정 양상을 관찰한 결과, 재광화용액 처리 후 NaF군은 법랑질 표면층에 구형의 결정이 형성되었고, BS+NaF군은 NaF군보다 표면층의 구형이 조밀하고, 법랑질 표면 하방의 격자 간격이 더욱 좁아졌으며, 법랑질 결정 사이의 미세공극이 채워져 있는 양상을 보였다.
2.법랑질 표면하방의 경도를 측정한 결과, 법랑질 표면하방 80 µm 깊이까지 총 VHN 변화값은 BS+NaF군(22.16)과 NaF군(18.87)이 BS군(11.57) 보다 통계적으로 유의하게 높게 증가하였다(p<0.001). 군간 깊이에 따른 경도의 변화는 5 µm 깊이에서는 NaF군이 27.87 로 다른 두 군에 비하여 통계적으로 유의하게 증가되었지만(p<0.01), 50 µm와 80 µm 깊이에서는 BS+NaF군이 각각 34.06과 18.06으로 NaF군과 BS군의 경도 증가량 보다 통계적으로 유의하게 높게 증가한 결과를 보였다(p<0.01, p<0.001).
이상의 연구결과에서 죽염과 불소를 혼합하여 사용한 경우 죽염은 초기우식법랑질 표면하방의 경도를 증가시켜 재광화 효과가 있으리라 사료된다.